在过去的几十年中,生物3D打印已被广泛地应用于构建如皮肤、血管、心脏等诸多组织/器官原型,,这不仅为器官替换的宏伟目标奠定基础,也可作为体外病理模型服务于药物筛选、器官发育及病变等领域。考虑到器官/组织有复杂的结构,种类繁多的生物3D打印方法被开发出来用以针对不同的应用场景。如何根据应用需求来选择合适的生物打印方法?本综述中我们系统地回顾了生物3D打印的发展、工艺流程和分类,重点介绍了打印的基本原理和商业化的生物打印设备;对挤出式、液滴式和光固化式生物3D打印进行了总结和分类,并对其应用提出了建议;我们认为未来比较会广泛应用的三个生物3D打印技术是投影式光固化打印、悬浮支撑打印及同轴打印;而设计生物墨水的要点是在可打印性、生物相容性和机械性能三者中找到平衡点。
相关综述以题为“Development of 3D Bioprinting: FromPrinting Methods to Biomedical Applications”被Asian Journalof Pharmaceutical Sciences在线刊登,顾则明博士生为一作,贺永教授为通讯作者。
我们认为:生物3D打印技术仍有着很大的进步空间。组织/器官的复杂程度给精确的生物打印带来了很大的困难,为解决这一问题,多尺寸、多材料、多细胞的生物打印将成为未来发展的重点。与天然组织/器官相比,生物打印的精度较低,这是目前生物打印技术的主要缺点之一。而另一个常见缺点是大尺寸复杂结构的打印速度慢,特别是涉及到多材料交替打印。此外,作为生物3D打印关键应用的体外组织模型不仅在尺寸上需要标准化,在生物相容性能和力学性能上也需要标准化,这就对生物打印技术的均匀性和再现性提出了更高的要求。相较于其他打印方法,投影式光固化生物3D打印技术在这些方面有着不小的优势。生物墨水的开发和应用是生物打印技术的关键。研究开发并稳定合成能够平衡可打印性、生物相容性和机械性能这三方面的新型生物墨水是生物3D打印应用的基础。目前的许多研究仍局限于使用有限范围的生物材料,而大多数人体组织/器官都有ECM成分的复杂组合,具有特定的生物学或力学影响,单一的生物墨水不可能建立一个“合成”的微环境来模拟体内的实际情况,这也使得多材料生物打印日益重要。血管化是生物打印活体结构的基础。与组织工程和再生医学领域面临的挑战一样,确保打印结构充分的血管化是生物3D打印的关键因素。有效构建多尺度的灌注血管网络,通过机械或化学刺激促进其血管化,是生物制造放大组织的基础。虽然建立血管网络的方法有多种,但每种方法都有其局限性,如喷墨生物打印和实验室打印分辨率高,但难以构建复杂的血管网络;基于牺牲材料的生物打印需要一个复杂的二次成型过程;同轴生物打印具有构建多尺寸流道的可行性和灌注培养的能力,在血管化领域有着广阔的应用前景。实现功能化是生物3D打印的首要目标。目前的大多数研究仍集中在打印过程和机制,这是面向制造业的想法,而生物3D打印功能化的核心因素是要从基础研究到实际应用。为实现功能化,生物墨水需要具备良好的生物相容性和力学性能,以满足营养灌注和植入的要求。同时,构建模拟体内微环境的场景,包括力学和化学刺激,对打印结构的功能化也至关重要。
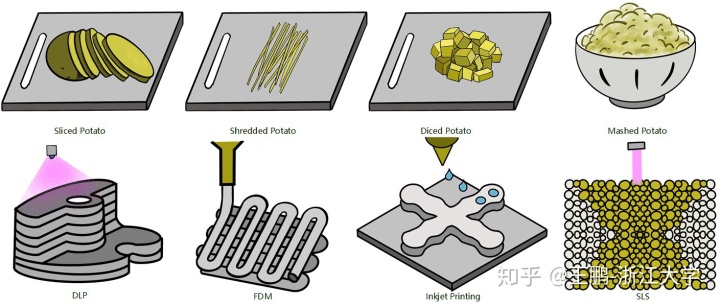
3D打印就好比切土豆的逆过程,切土豆是将土豆加工成土豆片、土豆丝、土豆丁或土豆泥,而3D打印则是将土豆片、土豆丝、土豆丁或土豆泥反向组装成土豆的过程,这四个过程就对应了四种典型的3D打印工艺:采用投影光固化组装的数字光处理(DLP)、采用纤维堆叠组装的熔融沉积(FDM)、采用微球进行组装的喷墨打印以及采用粉末烧结进行组装的选择性激光烧结(SLS)(图1)。
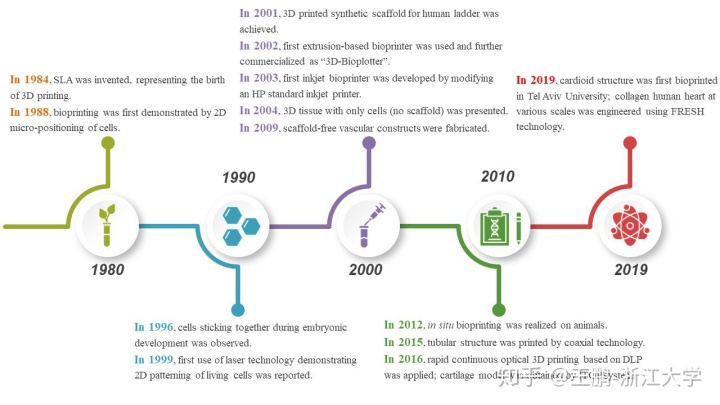
而生物3D打印是一门与机械、材料、生物、医学等多学科紧密相关的前沿技术。从广义上来说,直接为生物医疗领域服务的3D打印都可视为生物3D打印的范畴,而从狭义上来定义,通常将操纵含细胞生物墨水构造活性结构的过程称之为生物3D 打印,此概念也可称之为细胞打印。我们系统总结了生物3D打印的发展历程(图2)和工艺流程(图3)。

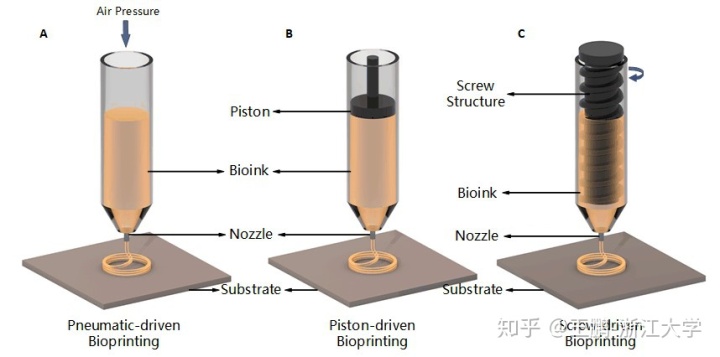
根据不同的打印原理和打印材料,我们整理了生物3D打印的分类,把常见的生物3D打印方法分为了挤出式、液滴式、光固化式三类。简单来说,挤出式生物打印通过挤出生物墨水形成连续纤维来搭建结构;液滴式生物打印生成离散液滴堆积成型;光固化生物打印利用光敏材料进行光固化并逐层堆叠,实现三维模型。挤出式生物打印可根据不同的出液方式,分为气动挤出式、活塞挤出式和螺旋挤出式三种(图4)。
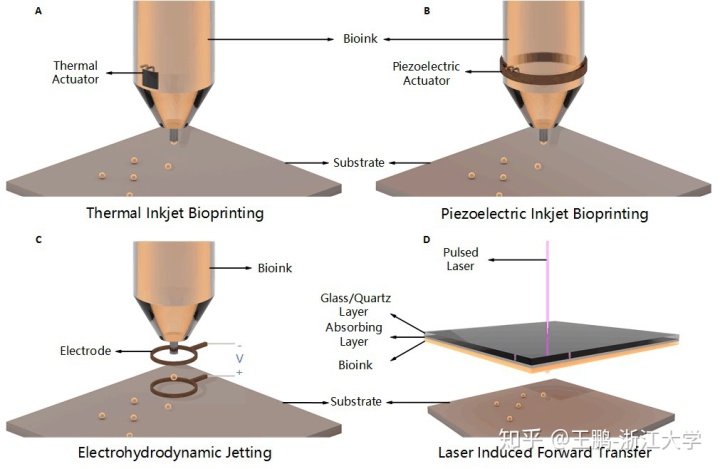
依据不同的液滴成形原理,我们可以把液滴式生物打印分为喷墨式、电流体动力喷射式(EHDJ)和激光辅助式(LAB)等。这其中,喷墨式生物打印常见的有热泡式、压电式等,而激光辅助式生物打印又可细分为激光引导直写(LGDW)和激光诱导前移(LIFT)(图5)。
光固化式生物打印可根据光扫描的方式不同分为立体光刻(SLA)和数字光处理(DLP)等。目前SLA技术在支架打印中应用较多,但在载细胞打印的应用并不多见。而DLP技术因其有着打印精度高、速度快、均一性好等优点越来越受到学术界的关注(图6)。
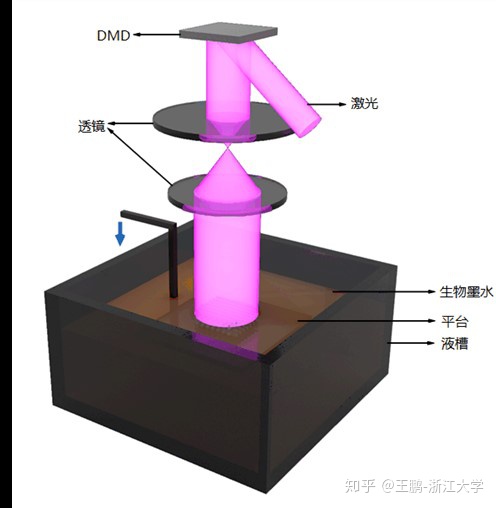
我们详细描绘了不同生物打印方法在生物医学领域的应用,包括在皮肤、骨/软骨、神经、肌肉/肌腱、脂肪、脊髓、血管/血管化、类器官、药物研究/肿瘤模型、临床应用等方面的研究现状,也总结概述了市场上知名的商业化生物打印设备,同时还对目前较为火热的多材料生物打印(图7)和同轴生物打印(图8)进行了细致的阐述。
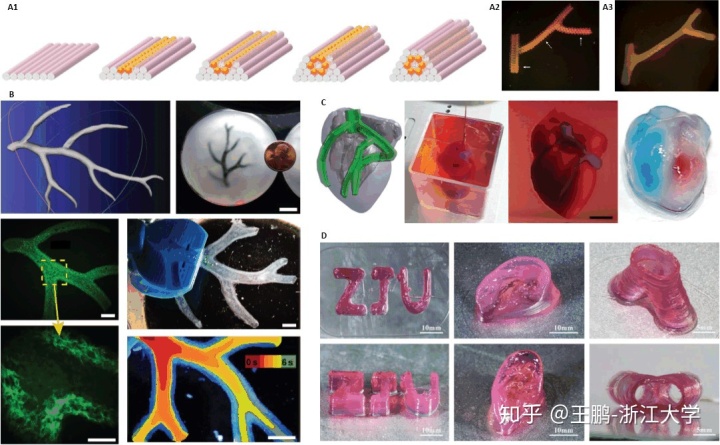
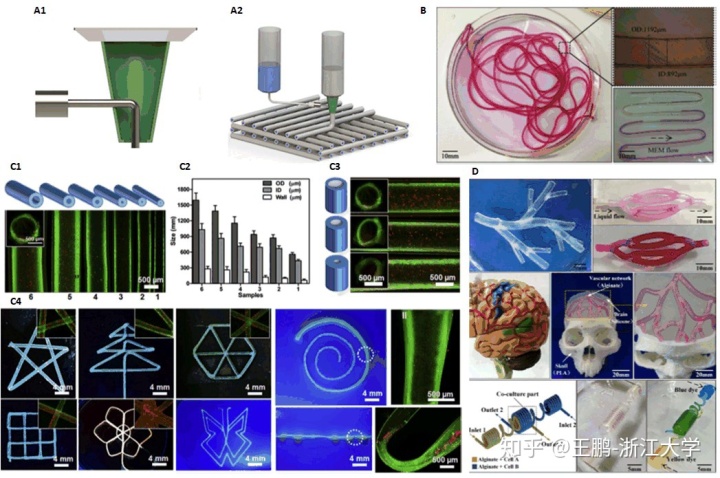
各种生物打印方法被发明出来用以针对不同的应用场景,相应地,每种生物打印方法也有着各自的优缺点。
挤出式生物打印是目前应用最为广泛的生物打印方法,其最大的优势在于可打印的生物相容材料范围广泛(包括细胞团、载细胞水凝胶、微载体、脱细胞基质成分等),涵盖了粘度范围从30mPa/s 到6×10^7mPa/s的生物材料,尤其是具有剪切变稀、快速交联特性的水凝胶材料。这意味着能为维持细胞活力和功能化提供合适微环境的低粘度材料,与能为打印结构提供力学支持的高粘度材料都能与挤出式生物打印很好地结合。同时,挤出式生物打印也有着良好的经济性和易用性等优点,与多材料、同轴生物打印可紧密结合。但挤出式生物打印也有着一些缺陷:首先,其打印精度相对其他生物打印方式较低,一般在100μm量级;其次,生物墨水的选择需要兼顾凝胶化、固化、剪切变稀等性质;此外,由于挤出过程中不可避免的剪切力可能会影响细胞存活率,这在打印细胞密度较高的生物墨水时更为明显。
喷墨式生物打印有着成本低、精度高、速度快等优点,也可针对性地配备多个喷嘴,以满足在同一时间打印不同的细胞、生物材料或生长因子的需求。然而,用于喷墨打印的生物墨水粘度要求限制了其适用生物材料的范围;由于驱动压力小,喷墨生物打印无法打印高粘度材料或高浓度细胞,用喷墨技术实现生理细胞密度的生物打印是目前比较困难的,而低粘度材料会降低打印成型的结构强度,导致不满足后续体外培养和移植的要求;此外,喷墨打印过程中可能会对细胞造成机械或热损伤,喷头也易损耗,这些缺点限制了喷墨生物打印技术的广泛应用。
激光辅助式生物打印相较于前两者有着一个先天优势:其无喷嘴的打印模式就避免了细胞/生物材料堵塞喷嘴的问题;同时这也避免了生物墨水与器件的直接接触,这种非接触式制造方法不会对细胞造成机械损伤。其打印高粘度生物墨水的生物材料选择范围比喷墨打印更广,打印精度甚至能达到生成含单个细胞的液滴。但激光辅助生物打印有几个明显的缺点:首先,成本相对较高,且缺乏商业化的打印设备,而适合激光生物打印的水凝胶材料并不多;其次,该方法自动化程度不高,如LIFT原理所述,每层墨水靠一次次涂层上去,不仅均一性得不到保证,且费时费力,导致其很难应用于复杂结构打印。
DLP是一种基于面投影的生物3D打印方法,相比应用广泛的挤出式打印有着更高的打印分辨率和可重复性。根据DLP的成型原理,它在打印速度上有很大的优势,因为无论结构多么复杂,每一层的打印时间都不会增加。此外,与喷墨生物打印中液滴之间、或挤出式打印的相邻纤维之间形成的“边界”相比,DLP技术可以更平滑地堆叠三维结构,从而大大提高了结构的完整性和力学性能。在光固化打印工艺中,未固化的液态生物墨水可以为打印结构提供良好的支撑,避免打印过程中水凝胶的坍塌变形;与LAB相同,无喷嘴的打印模式使得喷嘴堵塞、剪切力影响细胞活性等问题不再是困扰。我们认为,光固化生物打印技术将在细胞生物打印技术中发挥越来越重要的作用,有望取代挤出式生物打印成为未来最为主流的生物3D打印技术。
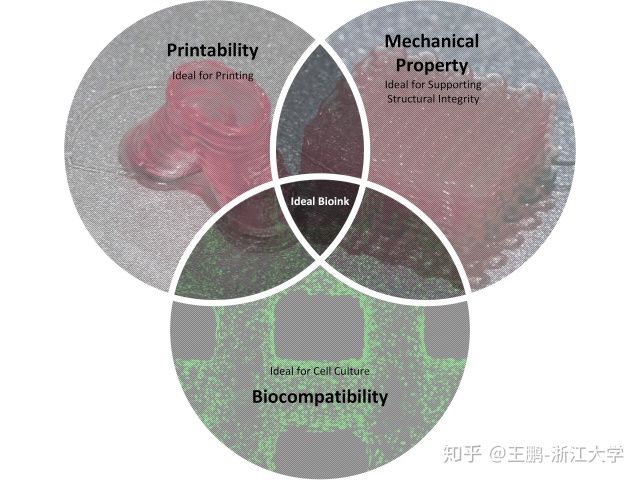
而生物墨水的性能大致可从三个方面予以评价:可打印性、生物相容性和机械性能(图9)。可打印性是评估生物墨水的可成型性,包括可调节的生物材料粘度、从溶胶态到凝胶态的快速转换性质,以及大范围的可打印参数等。生物相容性要求生物墨水尽可能地与人体中细胞微环境相似,使细胞在其中增殖、扩展、分化并交互。机械性能要求凝胶态的生物墨水力学性能够强,以支持随后的培养和植入过程;生物打印的结构通常需要在体外培养,在此期间常常伴随着营养物质的灌注和降解,需要相当的强度支持;机械性能不足也会导致移植失败。
论文链接:https://doi.org/10.1016/j.ajps.2019.11.003
本文转载自微信公众号“EngineeringForLife” 图文 | EFL 编辑 | 王鹏
